在實驗室內純化碳化合物,所需的基本提純方法包括:
蒸餾法;
分餾法;
液液萃取法和;
再結晶法。
我們之前已經對蒸餾法和分餾法有一定的了解(例如:石油的分餾),因此本小節重點介紹液液萃取法和再結晶法。
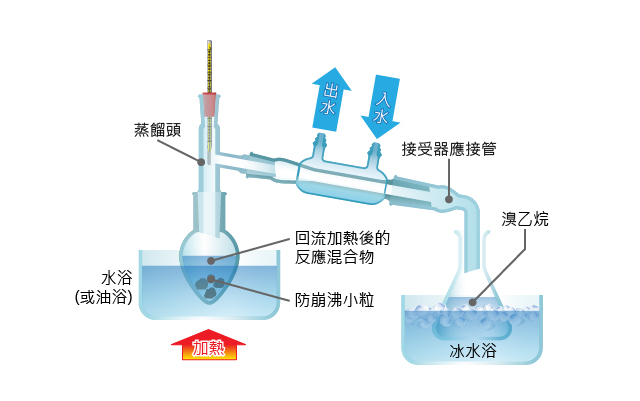
不同的化合物有不同的沸點,當液體混合物受熱時,沸點最低的液體率先變成氣體,沸點最高的液體則最後才變成氣體。蒸餾法就是運用這個原理把液體生成物從液體混合物中分離。一般而言,我們會在試劑或副生成物不易揮發的情況下才選擇蒸餾法,如乙醇和溴化氫在回流加熱後生成溴乙烷和水。

完成反應後,反應瓶內只有溴乙烷和水,溴乙烷的沸點是 \(38.4\; ^\circ \rm{C}\),水的沸點是 \(100\; ^\circ \rm{C}\)。可見,溴乙烷很容易被分離。
當生成物的沸點較低(低於 \(100\; ^\circ \rm{C}\)),可選用水浴;生成物的沸點較高(高於 \(100\; ^\circ \rm{C}\)),則選用油浴。透過水浴和油浴加熱反應瓶,可使熱力均衡傳入反應混合物。
分餾法的基本原理和蒸餾法相同,即利用化合物各有不同的沸點,透過「受熱氣化,冷卻液化」,把液體混合物中的成份逐一分離。即使是由互溶液體組成的混合物,亦可透過分餾法把每種混合物分離。
以下影片就以乙醇和丙\(-1-\)醇的混合物為例,說明分餾法的運作原理。
在製造碳化合物的過程中,經常要在不同階段使用水溶液和與水不互溶的有機溶劑。因此在提純時,我們免不了要把生成物從帶離子的水溶液(如氫氧化鈉和氯化鈉)中分離。在有機化合物的提純中,液液萃取法可把生成物從水溶液轉移至有機溶劑。
以下就以 \(1-\)氯戊烷為例,透過液液萃取法,把 \(1-\)氯戊烷從水溶液轉移至有機溶劑(例如乙氧基乙烷)中。
在常溫常壓下,很多有機化合物都是固體,例如苯甲酸。一般而言,從有機合成獲得的粗固體生成物都帶有少量雜質,因此我們會以再結晶法來進行提純。