氧化反應是醇的其中一個典型化學反應。在醇的氧化反應中,分子獲得氧原子或失去氫原子,生成含羰的生成物。
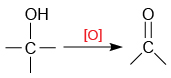
大部分的醇與氧化劑共熱時,產生氧化反應,生成醛、酮或羧酸;與之相反,醛、酮或羧酸與還原劑共熱時,產生還原反應,生成醇。本節,我們先討論氧化反應,還原反應則在其他課題討論。
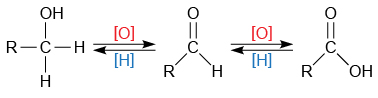
常見的氧化劑包括酸化重鉻酸鉀溶液 \(\text{(}{{\text{K}}_{\text{2}}}\text{C}{{\text{r}}_{\text{2}}}{{\text{O}}_{\text{7}}}\text{/}{{\text{H}}^{\text{+}}}\text{)}\) 及酸化高錳酸鉀溶液 \(\text{(KMn}{{\text{O}}_{\text{4}}}\text{/}{{\text{H}}^{\text{+}}}\text{)}\)。
例如:乙醇與酸化重鉻酸鉀溶液產生氧化反應,生成乙醛和水,反應混合物由橙色轉變成綠色。
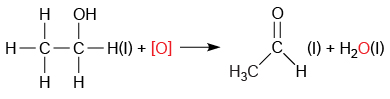
一級醇、二級醇和三級醇與氧化劑共熱時有不同的反應,生成醛、酮或酸,又或是不反應。
觀看影片了解它們的分別。
甲醇是最簡單的醇,它不屬於一級醇、二級醇或三級醇。根據不同的反應條件,甲醇與氧化劑產生氧化反應,生成甲醛、甲酸,甚至是二氧化碳。
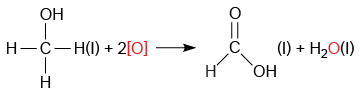
甲醇與氧化劑(例如酸化的重鉻酸鉀溶液)反應,生成甲醛和水。
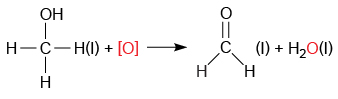
甲醇與輕微過量的氧化劑(例如酸化的重鉻酸鉀溶液)反應,生成甲酸和水。
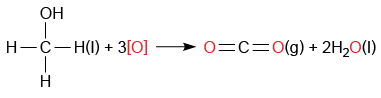
當甲醇與過量的氧化劑(例如酸化的重鉻酸鉀溶液)反應,最終會生成二氧化碳和水。
以下就以乙醇與酸化重鉻酸鉀溶液的氧化反應為例,說明醇與氧化劑的實驗裝置。
為什麼當乙醇轉化為乙醛時,我們可在同一個實驗裝置內把乙醇氧化,並且把乙醛從反應混合物中蒸餾分離?但當乙醇轉化為乙酸時,卻要兩個不同的實驗裝置?
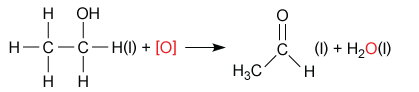
在乙醇轉化為乙醛的反應中,我們要避免乙醛氧化為乙酸,而乙醛(生成物)的沸點比乙醇(反應物)的沸點低,因此當加熱反應混合物時,乙醛會先被蒸餾出來;
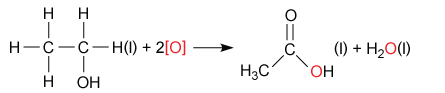
在乙醇轉化為乙醛的反應中,乙酸不會再被氧化,因此可在反應瓶內回流加熱,直至反應完成;而且乙醇(反應物)的沸點比乙酸(生成物)的沸點低,為了避免反應物逸走,因此不應在反應完成前進行蒸餾。