烴含有極之豐富的化學能,而我們可以通過燃燒,把烴的化學能轉化成光能及熱能。

發電機就是利用燃燒烴時釋放的熱能,把水加熱至沸點,形成水蒸氣,繼而推動渦輪,最後產生電能。

燃料燃燒時會與氧氣反應,氧氣通常來自空氣。
石油主要由烴組成,在氧氣充足的情況下,烴會完全燃燒,生成二氧化碳及水。
我們就以燃燒乙烷(脂肪族烴的一員)為例,說明烴的完全燃燒:
\(\ce{2C2H6(g) + 7O2(g) \to 4CO2(g) + 6H2O(l)}\)
根據以上的化學式,\(2\) 摩爾的乙烷須要 \(7\) 摩爾的氧氣方能完全燃燒。
燃料在燃燒時會釋放出大量的熱能,反應稱為放熱反應。在反應過程中,反應混合物的溫度會上升。
放熱反應釋放熱能,燃燒就是一個最常應用的例子,人們透過燃燒來煮食和取暖。

吸熱反應在反應過程中從環境中吸收熱能。
冰雪融化就是一個常見的吸熱過程,因此在大雪過後,室外溫度會比下雪時更低。

在氧氣不足的情況下,烴未能進行完全燃燒,因而產生一氧化碳及懸浮粒子。
以燃燒乙烷為例,說明烴的不完全燃燒:
\(\ce{2C2H6(g) + 5O2(g) \to 4CO(g) + 6H2O(l)}\)
在氧氣充足時,\(2\) 摩爾的乙烷跟 \(7\) 摩爾的氧氣進行完全燃燒,生成二氧化碳和水。但在氧氣不足的情況下,\(2\) 摩爾的乙烷會跟 \(5\) 摩爾的氧氣燃燒,生成一氧化碳和水;此外,\(2\) 摩爾的乙烷會跟 \(3\) 摩爾的氧氣燃燒,生成黑色的碳粒和水。
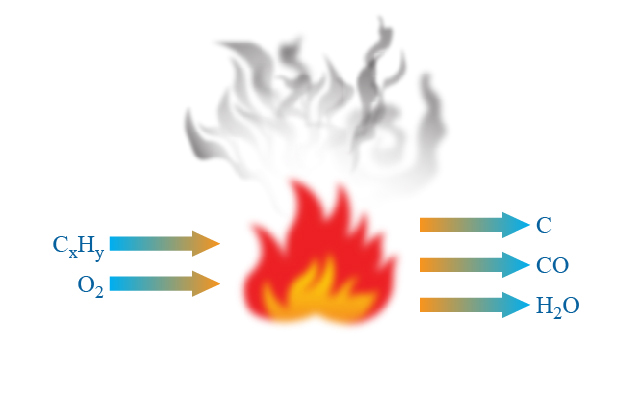
在火警發生時,我們所見到的黑色濃煙,是由於燃料不完全燃燒所產生。
烴分子內的碳原子愈多,烴便愈難完全燃燒,燃燒時會產生黃色火焰和放出黑煙。

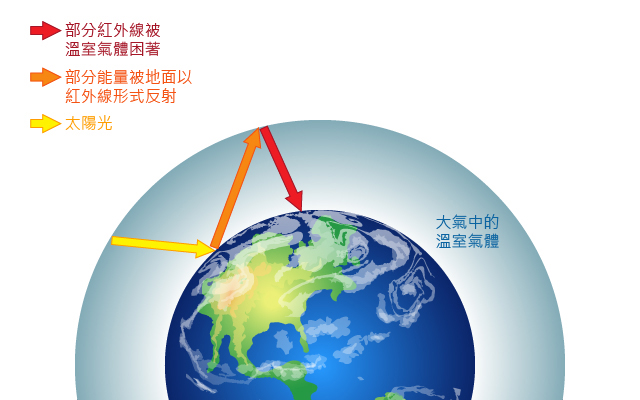
化石燃料在完全燃燒時會產生二氧化碳和水,而二氧化碳是最為人熟悉的溫室氣體。溫室是甚麼?溫室氣體又是甚麼呢?
溫室主要是由玻璃建成,它的特點就是要容許大量陽光進入室內,同時令室內保持溫暖,因此多用於室內種植促進植物生長。陽光會先透過玻璃進入溫室,但每當陽光經反射要離開溫室時,溫室的玻璃會將部分的紅外光反射到室內,令溫室保持溫暖。

地球的表面被大氣包圖,而大氣中的溫室氣體就扮演溫室中的玻璃,把要逃離地球表面的紅外光反射回大氣,把紅外光困著,令地球保持溫暖,這就是溫室效應。
如果沒有溫室效應,地球的表面溫度推測只有攝氏負十八度,生物會因為溫度太低而無法生存。
但自從工業革命開始,人類不斷燃燒化石燃料,把大量的二氧化碳釋放到大氣中,多於大自然的自然消耗量,使大氣中二氧化碳的濃度不斷增加,從而困著愈來愈多的紅外光,令地球表面的溫度不斷上升。
其他溫室氣體包括甲烷、氯氟碳類化合物(\(\ce{CFCs}\))和氮氧化物。