從理論層面而言,無論是瞬時速率,還是平均速率,其實都是在量度這個反應在某一時段內(即是某兩個時點之間)反應物/生成物濃度的變化。
因此,透過實驗方法找出反應速率必須記錄反應物/生成物濃度及相應的時間。
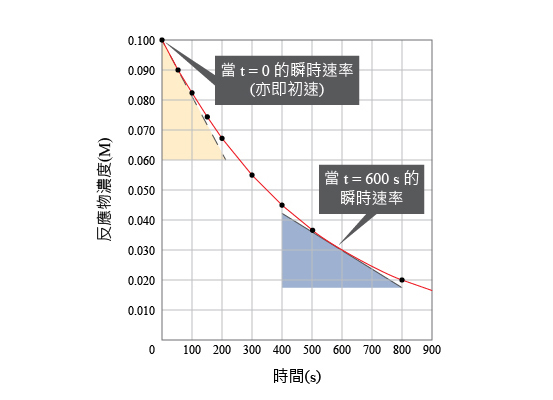
我們在量度反應速率時,有些方面必須注意。
由於反應速率是反應物(或生成物)濃度隨著時間的變化,因此我們要量度反應物(或生成物)的濃度和時間。
由於溫度對反應速率有決定性的影響,因此反應必須在恆溫的環境下進行。
當我們量度反應速率時,要避免影響反應的進度。例如一個化學反應大約需要 \(1\) 個小時完成,若果我們每次都把反應停止來量度反應速率,那麼實驗結果便會很容易出現誤差。
滴定法是其中一種常用來量度反應速率的方法。
但要留意,當我們從反應混合物中抽取定量的樣本進行滴定分析時,由於分析需時,為了減少誤差,我們必須把反應停止(或減慢反應速率)。
以下是一些常用來減慢反應速率的方法:
以冰凍樣本混合物降溫。(如果反應混合物跟水產生化學反應,則要用冰浴進行冰鎮;如果反應混合物不會跟水產生化學反應,則可直接加入冰水。)
移除催化劑。
加入另一種反應物(過量而且定量),使之與原來的反應物反應,直至耗盡。
加入大量凍水把樣本稀釋。
當我們用滴定法採集樣本時,我們要盡量避免影響反應進度,而且採集樣本要定時定量。
我們可選用合適體積的移液管,從反應混合物中抽取樣本。
以下是一些常用來減慢反應速率的方法:
以冰凍樣本混合物降溫。(如果反應混合物跟水產生化學反應,則要用冰浴進行冰鎮;如果反應混合物不會跟水產生化學反應,則可直接加入冰水。)
移除催化劑。
加入另一種反應物(過量而且定量),使之與原來的反應物反應,直至耗盡。
加入大量凍水把樣本稀釋。