紅外光譜法 (Infrared spectroscopy,簡稱 IR) 是化學家最為常用的光譜技術之一,它量度的是樣本對不同頻率的紅外光的吸收度。
紅外光能改變分子的振動能量。我們已經知道,只有與化學物種發生能級躍遷所需能量相吻合的輻射,才會被該化學物種吸收。分子對紅外光的吸收亦不例外。只有與分子中某個化學鍵發生振動能級躍遷所需能量相吻合的紅外光,才會被吸收,令該化學鍵由振動基態 (能量最低的振動能級) 躍遷至激發態 (能量較高的振動能級)。
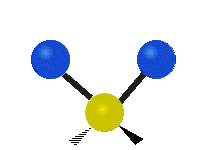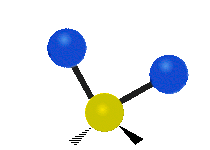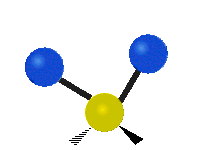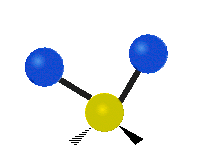
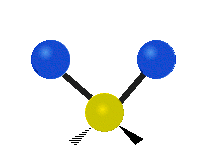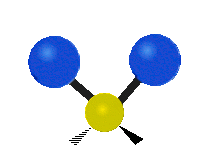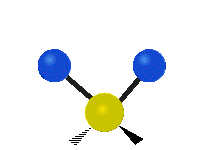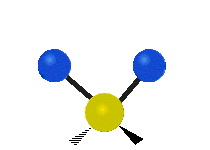
結構簡單的雙原子分子 (如 \(\ce{HCl}\) 等) 的振動模式只有伸縮振動,較複雜的分子或基團 (如 \(\ce{- CH2 -}\) 等) 的振動模式則較為複雜,包括多種不同的伸縮振動和彎曲振動。
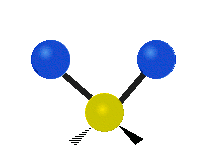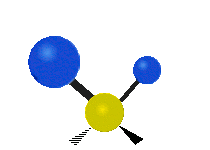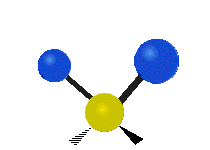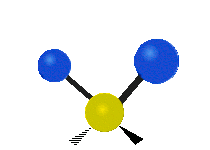
| 對稱伸縮 | 不對稱伸縮 | 剪式振動 |
|---|---|---|
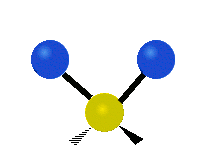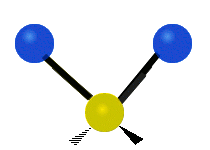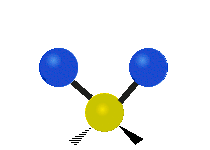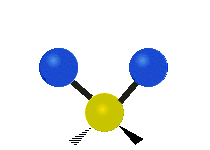 |
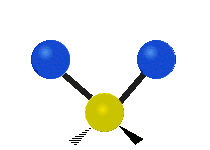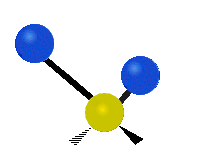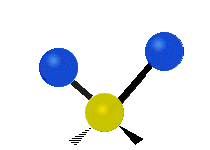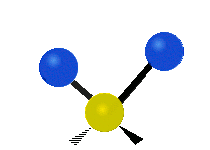 |
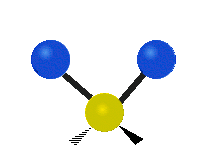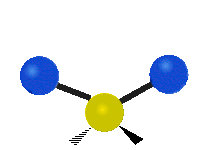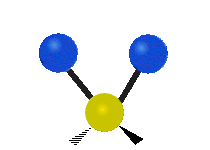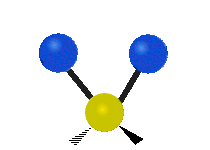 |
| 左右搖擺振動 | 上下搖擺振動 | 扭轉振動 |
 |
 |
 |
不同的化學鍵,在發生振動能級躍遷時,所吸收的紅外光的頻率有所不同。這主要與化學鍵的組成和強度有關。以共價鍵的伸縮振動為例,一般而言,
若共價鍵的強度愈高,它在發生能級躍遷時所吸收的紅外光的頻率愈高。例如,雙鍵的強度高於單鍵,因此在發生振動能級躍遷時,\(\ce{C=O}\) 所吸收的紅外光的頻率明顯高於 \(\ce{C-O}\)。
若構成共價鍵的原子的質量愈大,該共價鍵在發生能級躍遷時所吸收的紅外光的頻率愈低。例如,鹵素原子的質量由 \(\ce{F}\) 至 \(\ce{I}\) 逐漸增大,因此在發生振動能級躍遷時,\(\ce{C-X}\) 所吸收的紅外光的頻率逐漸降低。
| 共價鍵 | 與伸縮振動相關的吸收波數區域 \((\text{cm}^{-1})\) |
|---|---|
| \(\ce{C=O}\) | \(1680-1750\) |
| \(\ce{C-O}\) | \(1000-1300\) |
| 共價鍵 | 與伸縮振動相關的吸收波數區域 \((\text{cm}^{-1})\) |
|---|---|
| \(\ce{C-F}\) | \(1000-1400\) |
| \(\ce{C-Cl}\) | \(600-800\) |
| \(\ce{C-Br}\) | \(500-600\) |
| \(\ce{C-I}\) | \(490-620\) |
正因為不同的化學鍵吸收不同頻率的紅外光,因此,用紅外光照射樣本時,樣本只會吸收其中一部分,而其餘的則不會被吸收,直接穿過樣本。利用紅外光譜儀,可以探測和記錄樣本對不同頻率的紅外光的吸收情況,並將其繪製成圖表,即該樣本的紅外光譜。根據紅外光譜,化學家可推斷碳化合物中所含的化學鍵和官能基,從而辨識碳化合物和推斷碳化合物的結構。
