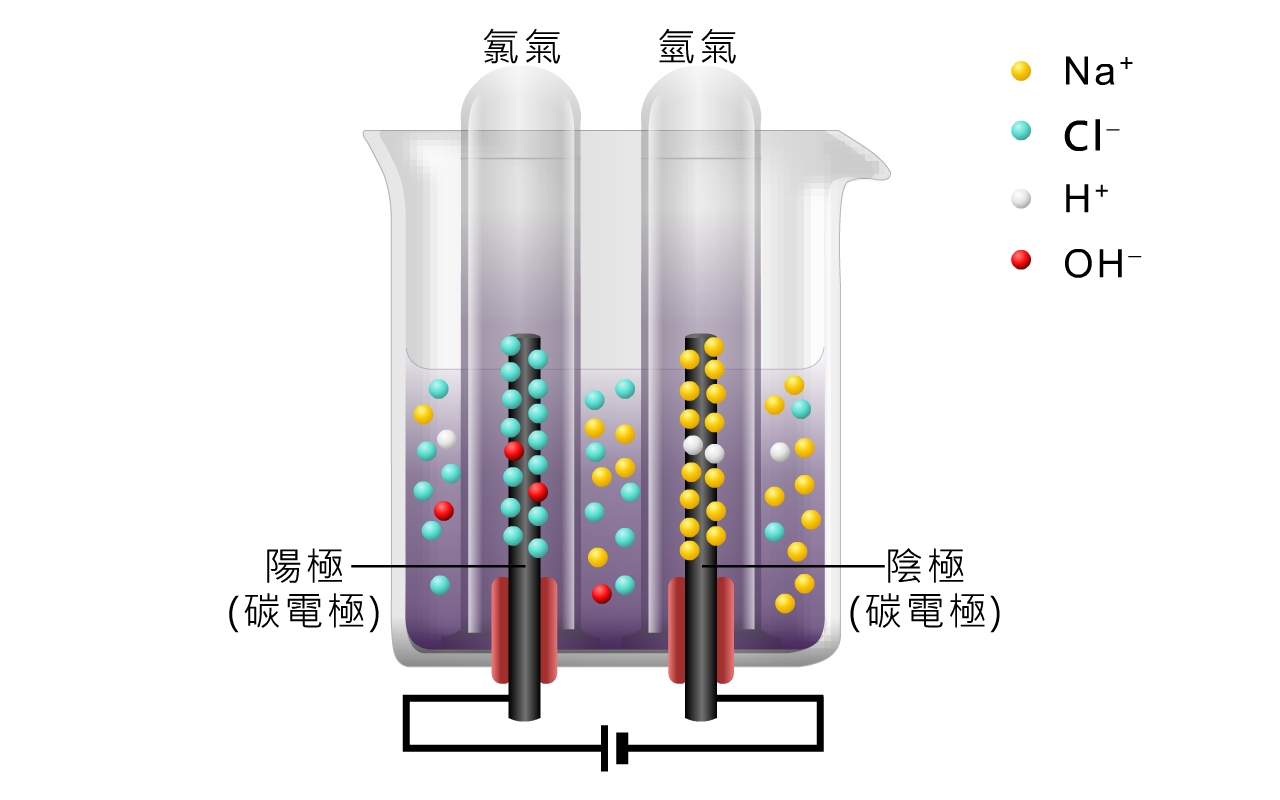
離子在溶液中的濃度,可能會影響離子的優先放電次序。
一般而言,在溶液中濃度較高的離子,較容易放電。特別地,若在同一電極上的不同離子在電化序中的位置相差不大,濃度高出很多的離子則會優先放電。
例如,在電解極稀氯化鈉溶液時,溶液中的 \(\ce{Cl^- (aq)} \) 和 \(\ce{OH^- (aq)} \) 的濃度相近。由於 \(\ce{OH^- (aq)} \) 在電化序中的位置較高,因此 \(\ce{OH^- (aq)} \) 優先放電。然而,在電解濃氯化鈉溶液時,由於溶液中的 \(\ce{Cl^- (aq)} \) 濃度遠高於 \(\ce{OH^- (aq)} \),且兩種離子在電化序中的位置相距不遠,濃度效應導致 \(\ce{Cl^- (aq)} \) 優先放電。