比較化學電池和電解池的異同,將你的答案填入下表中。
化學電池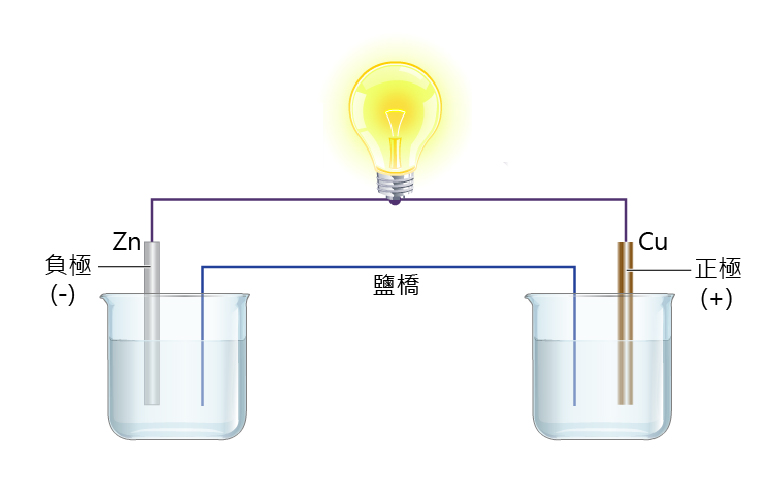
|
電解池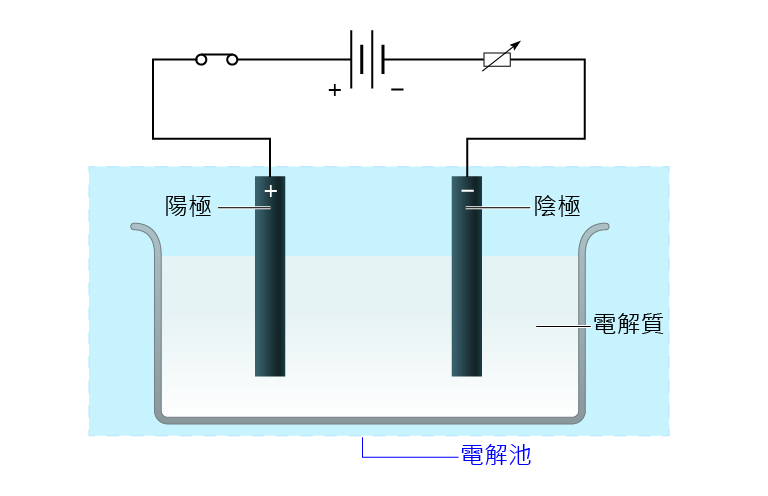
|
||
|---|---|---|---|
| 能量轉換 |
將
|
將
|
|
| 涉及的化學反應 |
|
|
|
| 電極的性質以及電極上發生的化學反應 | 正電極 (+) |
發生 |
發生 |
| 負電極 (−) |
發生 |
發生 |
|
簡單化學電池與電解池中發生的能量轉換過程剛好相反。簡單化學電池是利用化學反應產生電能的裝置,因此在簡單化學電池中,化學能轉化為電能。然而,電解池則是由電能引發化學反應的裝置,因此在電解池中,電能轉化為化學能。
簡單化學電池和電解池內發生的均是氧化還原反應。但是,簡單化學電池內的反應是自發進行的,而電解池內的反應卻是在外加電力的迫使下發生的。
化學電池的正負電極,是根據電子流動的方向來分辨的。有電子流出的電極是負電極,電子流入的電極是正電極。在簡單化學電池中,電子從活潑金屬電極流出,經外電路流向不活潑金屬電極。所以,活潑金屬電極是負電極,不活潑金屬電極是正電極。然而,電解池中的兩個電極是與外接電源的正負極相連接的,與外加電源負極相連的電極,被迫帶上負電荷,成為負電極,與外加電源正極相連的電極上被迫帶上正電荷,成為正電極。
不論是化學電池還是電解池,分辨陽極和陰極的方法均相同。發生氧化反應的電極是陽極,發生還原反應的電極則是陰極。
對比簡單化學電池和電解池的正負極和陰陽極,你會發現:簡單化學電池的負電極是陽極,而電解池的負電極是陰極; 簡單化學電池的正電極是陰極,而電解池的正電極是陽極。