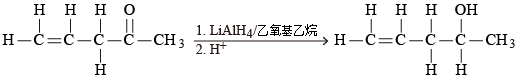碳化合物的氧化反應和還原反應的關係密不可分:反方向的氧化反應就是還原反應。
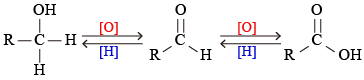
一般而言,碳化合物的氧化反應是指分子內的含氧量上升或含氫量下降;還原反應是指分子內的含氧量下降或含氫量上升。
分子內的含氧量上升並不代表分子被氧化,例如鹵烷的水解中,鹵烷轉化為醇。雖然分子內含氧量上升,但這不是氧化反應。
丙酸可被還原為丙醛,而丙醛可被還原為丙\(-1-\)醇。試用化學試描述。
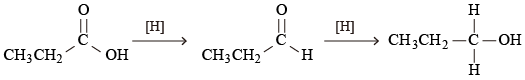
小知識:要判斷某化學反應是否氧化/還原反應,重點在於反應物內的任何一個原子有否涉及氧化數的轉變。
在實驗室中,常見的還原劑包括四氫合鋁酸鋰 \(\text{LiAl}{{\text{H}}_{\text{4}}}\) 和四氫合硼酸鈉 \(\text{NaB}{{\text{H}}_{\text{4}}}\)。
四氫合鋁酸鋰可還原多種有機化合物,例如醛、酮、羧酸和醚;四氫合硼酸鈉多應用於醛和酮的還原反應。
四氫合鋁酸鋰是非常活潑的還原劑,它與醛和酮的反應非常劇烈;四氫合硼酸鈉則是較溫和的還原劑。
例如:丙醛被四氫合鋁酸鋰還原為丙\(-1-\)醇。
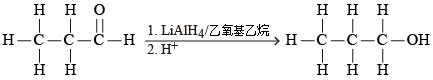
除了作為還原劑,四氫合鋁酸鋰和四氫合硼酸鈉亦會與水(或酸)產生反應。
四氫合鋁酸鋰與水產生劇烈反應,生成氫氣。因此當使用四氫合鋁酸鋰為還原劑時要避免與水接觸。
\(\text{LiAl}{{\text{H}}_{\text{4}}}\text{(s) + 4}{{\text{H}}_{\text{2}}}\text{O(l) }\xrightarrow{{}}\text{ LiOH(s) + Al(OH}{{\text{)}}_{\text{3}}}\text{(s) + 4}{{\text{H}}_{\text{2}}}\text{(g)}\)
而四氫合硼酸鈉與水的反應相對地緩慢,因此可先溶於鹼性的水溶液中,然後再與醛或酮反應。
\(\text{NaB}{{\text{H}}_{\text{4}}}\text{(s) + 2}{{\text{H}}_{\text{2}}}\text{O(l) }\xrightarrow{{}}\text{ NaB}{{\text{O}}_{\text{2}}}\text{(s) + 4}{{\text{H}}_{\text{2}}}\text{(g)}\)
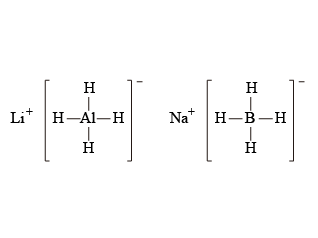
四氫合鋁酸鋰是非常活潑的還原劑,它與醛的反應非常劇烈,生成一級醇;四氫合硼酸鈉則是較溫和的還原劑。例如:丙醛被四氫合鋁酸鋰還原為丙\(-1-\)醇。
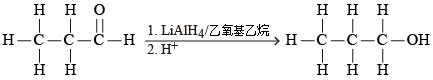
丙醛亦可被四氫合硼酸鈉還原為丙\(-1-\)醇。

還原劑 \(\text{LiAl}{{\text{H}}_{\text{4}}}\) 只會把羰基還原,不會影響碳\(-\)碳雙鍵,所以 \(\text{LiAl}{{\text{H}}_{\text{4}}}\) 可以把不飽和的醛轉化為不飽和的一級醇。

醛(或酮)的還原反應包括兩個步驟:
把醛加入溶於無水的乙氧基乙烷的四氫合鋁酸鋰溶液中;
完成第 1 步後,把稀釋的酸性溶液加入反應混合物內。
為甚麼還原反應要分為兩步進行?
在第 1 步中,醛 \(\text{(RCHO)}\) 與四氫合鋁酸鋰反應,生成烷氧基鋰 \(\text{(RC}{{\text{H}}_{\text{2}}}{{\text{O}}^{-}}\text{L}{{\text{i}}^{\text{+}}})\)。在第 2 步中,烷氧基鋰獲得氫離子,生成醇 \(\text{(RC}{{\text{H}}_{\text{2}}}\text{OH)}\)。
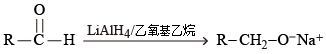
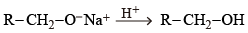
假若把醛加入稀釋的酸性溶液,反應混合物內同時存在氫離子 (\(\rm{H}^{+}\))、水分子 (\(\rm{H}_{2}\rm{O}\)) 和醛。四氫合鋁酸鋰會優先與氫離子和水分子反應,生成氫氣;在氫離子和水分子完全消耗完後,四氫合鋁酸鋰才與醛產生還原反應。因此還原反應要先以無水的乙氧基乙烷為溶劑,並分為兩步進行。
與醛的化學反應一樣,四氫合鋁酸鋰和四氫合硼酸鈉可把羰基還原為羥基,生成二級醇。例如:丙酮被四氫合鋁酸鋰還原為丙\(-2-\)醇。
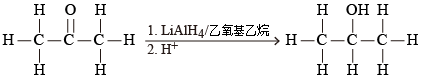
丙醛亦可被四氫合硼酸鈉還原為丙\(-2-\)醇。

還原劑\(\;\rm{LiAlH}_{4}\;\)只會把羰基還原,不會影響碳\(-\)碳雙鍵,所以\(\;\rm{LiAlH}_{4}\;\)可以把不飽和的酮轉化為不飽和的二級醇。