碳或惰性金屬(例如,鉑)也可以作為化學電池的電極。由於這類電極不會與電解質發生化學反應,因此稱為惰性電極。
含有惰性電極的化學電池是利用兩個半電池將氧化反應和還原反應分開,而電子則經過電極和導線在外電路流動。
通過右側的互動,學習含惰性電極的化學電池的組成及工作原理,並完成相應的題目。
點擊互動中左側的燒杯,觀察燒杯內溶液的變化,並回答下面的題目。
點擊互動中右側的燒杯,觀察燒杯內溶液的變化,並回答下面的題目。
根據兩個燒杯內的化學變化回答下面的問題。
該氧化還原過程的總反應式為:
\(\text{Mn}{{\text{O}}_{\text{4}}}^{-}\left( \text{aq} \right)\ \text{+}\ \) \({{\text{H}}^{\text{+}}}\left( \text{aq} \right)\ \text{+}\) \(\text{F}{{\text{e}}^{\text{2+}}}\left( \text{aq} \right)\ \) \( \to \ \) \(\text{M}{{\text{n}}^{\text{2+}}}\left( \text{aq} \right)\ \text{+}\ \) \({{\text{H}}_{\text{2}}}\text{O}\left( \text{l} \right)\ +\ \) \(\text{F}{{\text{e}}^{\text{3+}}}\left( \text{aq} \right)\)
通過互動中展示的含惰性電極的化學電池以及上面的分析,以下哪些描述是正確的?
電極本身不參與氧化還原反應
電化序上方的物種發生氧化反應;下方的物種發生還原反應
電化序上方的物種所在的電極是負極;下方的物種所在的電極是正極
兩個半電池的溶液混合時,亦可直接發生氧化還原反應
電池的本質是利用鹽橋或多孔裝置改良的簡單化學電池
通過前面的介紹可知:含惰性電極的化學電池,實際上就是用兩個半電池分別盛裝參與反應的氧化劑和還原劑,並用惰性電極(例如:碳或鉑)連接,從而達至電子的定向移動。
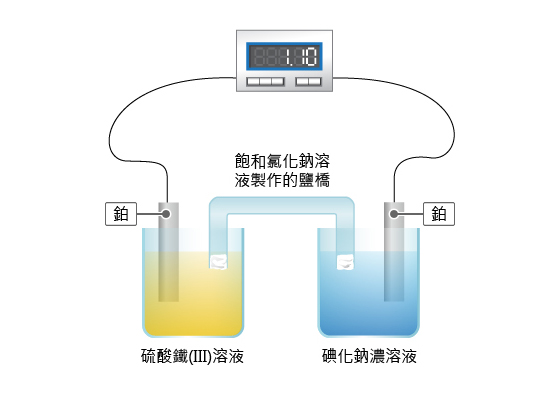
根據右側圖片展示的信息,回答下列問題。
關於右側所展示的化學電池,以下哪項/哪些描述是正確的?
可用碳代替鉑作為金屬電極
碘化鈉濃溶液所在的電極連接的是萬用表的負端鈕
硫酸鐵(III) 溶液獲得電子,發生的是還原反應
硫酸鐵(III) 溶液的顏色由棕黃色變為淡綠色
碘化鈉濃溶液所在的電極周圍會逐漸變為棕色
以下哪項離子半反應式可描述電池的正極所發生的化學變化?
\(\text{2}{{\text{I}}^{-}}\left( \text{aq} \right)\ \to \ {{\text{I}}_{\text{2}}}\left( \text{aq} \right)\ \text{+}\ \text{2}{{\text{e}}^{-}}\)
\(\text{S}{{\text{O}}_{\text{4}}}^{\text{2}-}\left( \text{aq} \right)\ \text{+}\ {{\text{H}}_{\text{2}}}\text{O}\left( \text{l} \right)\ \text{+}\ \text{2}{{\text{e}}^{-}}\ \to \ \text{S}{{\text{O}}_{\text{3}}}^{\text{2}-}\left( \text{aq} \right)\ \text{+}\ \text{2O}{{\text{H}}^{-}}\left( \text{aq} \right)\)
\(\text{F}{{\text{e}}^{\text{3+}}}\left( \text{aq} \right)\ \text{+}\ {{\text{e}}^{-}}\ \to \ \text{F}{{\text{e}}^{\text{2+}}}\left( \text{aq} \right)\)
\(\text{F}{{\text{e}}^{\text{3+}}}\left( \text{aq} \right)\ \text{+}\ \text{3}{{\text{e}}^{-}}\ \to \ \text{Fe}\left( \text{s} \right)\)
以下哪項離子半反應式可描述電池的負極所發生的化學變化?
\(\text{2}{{\text{I}}^{-}}\left( \text{aq} \right)\ \to \ {{\text{I}}_{\text{2}}}\left( \text{aq} \right)\ \text{+}\ \text{2}{{\text{e}}^{-}}\)
\(\text{S}{{\text{O}}_{\text{4}}}^{\text{2}-}\left( \text{aq} \right)\ \text{+}\ {{\text{H}}_{\text{2}}}\text{O}\left( \text{l} \right)\ \text{+}\ \text{2}{{\text{e}}^{-}}\ \to \ \text{S}{{\text{O}}_{\text{3}}}^{\text{2}-}\left( \text{aq} \right)\ \text{+}\ \text{2O}{{\text{H}}^{-}}\left( \text{aq} \right)\)
\(\text{F}{{\text{e}}^{\text{3+}}}\left( \text{aq} \right)\ \text{+}\ {{\text{e}}^{-}}\ \to \ \text{F}{{\text{e}}^{\text{2+}}}\left( \text{aq} \right)\)
\(\text{F}{{\text{e}}^{\text{3+}}}\left( \text{aq} \right)\ \text{+}\ \text{3}{{\text{e}}^{-}}\ \to \ \text{Fe}\left( \text{s} \right)\)
以下哪項反應式能夠正確描述化學電池內發生的氧化還原反應?
\(\text{SO}_{4}^{2-}( \text{aq} ) + 2\text{I}^{-}( \text{aq} ) + \text{H}_{2}\text{O}( \text{l} )\to \text{SO}_{3}^{2-}( \text{aq} ) + \text{I}_{2}( \text{aq} ) + 2\text{OH}^{-}( \text{aq} )\)
\(\text{2F}{{\text{e}}^{\text{3+}}}\left( \text{aq} \right)\ +\ \text{2}{{\text{I}}^{-}}\left( \text{aq} \right)\ \to \ 2\text{F}{{\text{e}}^{\text{2+}}}\left( \text{aq} \right)\ +\ {{\text{I}}_{\text{2}}}\left( \text{aq} \right)\)
\(\text{2F}{{\text{e}}^{\text{3+}}}\left( \text{aq} \right)\ +\ \text{6}{{\text{I}}^{-}}\left( \text{aq} \right)\ \to \ 2\text{Fe}\left( \text{s} \right)\ +\ 3{{\text{I}}_{\text{2}}}\left( \text{aq} \right)\)
關於鹽橋發生的變化,以下哪項/哪些描述是正確的?
鹽橋中的鈉離子,流向硫酸鐵(III) 溶液
鹽橋中的氯離子,流向碘化鈉濃溶液
生成的碘會流入鹽橋,使鹽橋變為棕色
生成的鐵(II) 離子會流入鹽橋,使鹽橋變為淡綠色
鐵(III) 離子會流入鹽橋,使鹽橋變為棕色